Tenside!
Der Begriff kommt vom Lateinischen „tendere” = Spannung. Fast jedes Reinigungsmittel und jede Pflegeemulsionen enthält diese Substanzen.
|
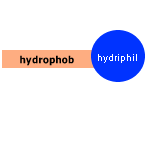
Was sind Tenside. Da sich Wasser und Öl nicht von alleine Mischt, helfen uns die sogenannten Tenside. Die Tenside bewirken, dass Fett sich im Wasser löst. Man Bezeichnet dies auch als WAS = „waschaktiven Substanzen“. In Reinigungsmitteln sind sie dafür zuständig, dass sich Fett von der Oberfläche löst und man die Verunreinigung entfernen kann. Die Tensidmolekül bestehen aus einem „wasserliebenden“ (hydrophilen) Kopf und einem „wasserabweisenden“ (hydrophoben) Schwanz. Die hydrophoben Enden lagern sich an Fett oder Verschmutzungen an, und es bildet am Material eine Art „Tensidhülle“. Die hydrophilen Enden verbinden sich mit dem Reinigungsflotte. So entstehen „Fetttröpfchen mit Tensidhüllen“ - die durch diesen Vorgang wasserlöslich werden. |
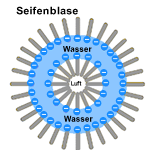
Entstehung von Seifenblasen:
|
Beim Schütteln des Reinigers dringt Luft in die Tensid-Lösung es entsteht eine Schaumblasen. Das Verhalten der Seifenmoleküle ist eng verbunden mit der Schaumbildung. Es bilden sich viele kleine Luftblasen. Diese werden von den Seifenmolekülen und durch die geringe Oberflächenspannung des sehr dünnen Wasserfilm umschlossen. Bei solchen Luftbläschen werden die die hydrophoben Enden der Seifenmoleküle sowohl nach innen als auch nach außen gerichtet. |
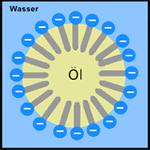
Fette werden wasserlöslich:
|
Treffen im Wasser befindliche Mizellen auf Fette oder Öle, richtet sich der hydrophobe Teil zum Fett aus. Der hydrophile Teil bleibt weiter im Wasser. Die Moleküle werden also zu einem Bindeglied zwischen Wasser und Fett. Auf diese Art wird fettiger Schmutz in Wasser gelöst. Über die verringerte Oberflächenspannung kann mit Tensiden angereichertes Wasser tief in verschmutztes Material eindringen und das Fett ablösen. |
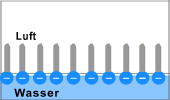
Oberflächenspannung des Wassers:
|
Tenside bilden an der Wasseroberfläche eine Schicht, die sehr dünn ist, es wird dadurch die Oberflächenspannung des Wassers herabgesetzt. Die hydrophilen Enden ragen in Richtung des Wassers, die hydrophoben Enden ragen in Richtung der Luft. |
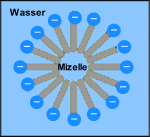
Mizelle im Wasser:
|
Die Tenside schließen sich hierbei zu Verbänden zusammen, wobei in einem polaren Lösungsmittel sich die unpolaren Schwänze der Tenside nach innen orientieren(siehe Abbildung).
Sie entgehen auf dieser Weise den Abstoßungskräften zum polaren Lösungsmittel. Im Innern der Micelle sorgen Van - der -Waals - Kräfte, Mit Van-der-Waals-Kräften, benannt nach dem niederländischen Physiker Johannes Diderik van der Waals (18371923) für den Zusammenhalt. |